Les actions de la firme biotechnologique se sont envolées à l'annonce de la réponse immunitaire décelée lors des essais de son vaccin ; les essais de Phase 3 débuteront en juillet...
Le médecin-chef de la firme biotechnologique Moderna a indiqué lundi que son vaccin expérimental contre la Covid-19 « s’avère fonctionner » après des tests réalisés sur un petit nombre de volontaires et que les essais de phase III, qui impliqueront plusieurs milliers de personnes, seront lancés au mois de juillet.
« Nous avons obtenu les premiers résultats aujourd’hui… et aujourd’hui, nous avons montré que [le vaccin] s’avère fonctionner… Nous avons été en mesure de stimuler le système immunitaire », a commenté lundi le docteur Tal Zaks.
 « Vers la fin de l’année ou le début de l’année prochaine, il existe une probabilité raisonnable de voir ce vaccin sur le marché, au moins sur le marché américain », a-t-il dit dans un entretien accordé à la Douzième chaîne depuis le siège de Moderna, dans le Massachusetts.
« Vers la fin de l’année ou le début de l’année prochaine, il existe une probabilité raisonnable de voir ce vaccin sur le marché, au moins sur le marché américain », a-t-il dit dans un entretien accordé à la Douzième chaîne depuis le siège de Moderna, dans le Massachusetts.
Le médecin-chef de Moderna, le docteur Tal Zaks (Capture d’écran : Douzième chaîne)
Il a expliqué que la bataille contre la Covid-19 marquait la neuvième tentative de la firme de développer des vaccins contre les virus « et nous sommes arrivés à nos fins lors des huit essais antérieurs ». Et ainsi, a-t-il ajouté, « le degré de confiance que nous saurons y arriver encore une fois au sein de l’entreprise » est également élevé aujourd’hui, a-t-il poursuivi.
Les informations portant sur les progrès réalisés par l’entreprise pharmaceutique – qui ont été rendues publiques dans un communiqué de presse lundi – ont fait grimper les actions de Moderna de plus de 22 %, et aidé à soutenir le marché boursier dans un sens plus large.

Un panneau marque l’entrée de Moderna, le 18 mai 2020, à Cambridge, dans le Massachussetts (Crédit : AP Photo/ Bill Sikes)
Moderna a annoncé que le vaccin en préparation, le mRNA-1273, avait entraîné une réponse immunitaire chez les huit personnes qui en ont été inoculées – une réponse similaire à celle des malades souffrant de la Covid-19.
Au cours de l’entretien, Tal Zaks a précisé qu’à sa dose la plus basse, le vaccin avait produit une réaction similaire à celle des patients se remettant « naturellement » de la maladie. À dosage moyen – de 100 microgrammes – il a créé « davantage d’anticorps » que ceux créés naturellement chez les individus ayant contracté la Covid-19.
Pour l’occasion, trois groupes de 15 patients âgés de 18 à 55 ans ont reçu différentes doses de vaccin dans les essais de phase I. Les résultats complets ne sont pas encore connus.
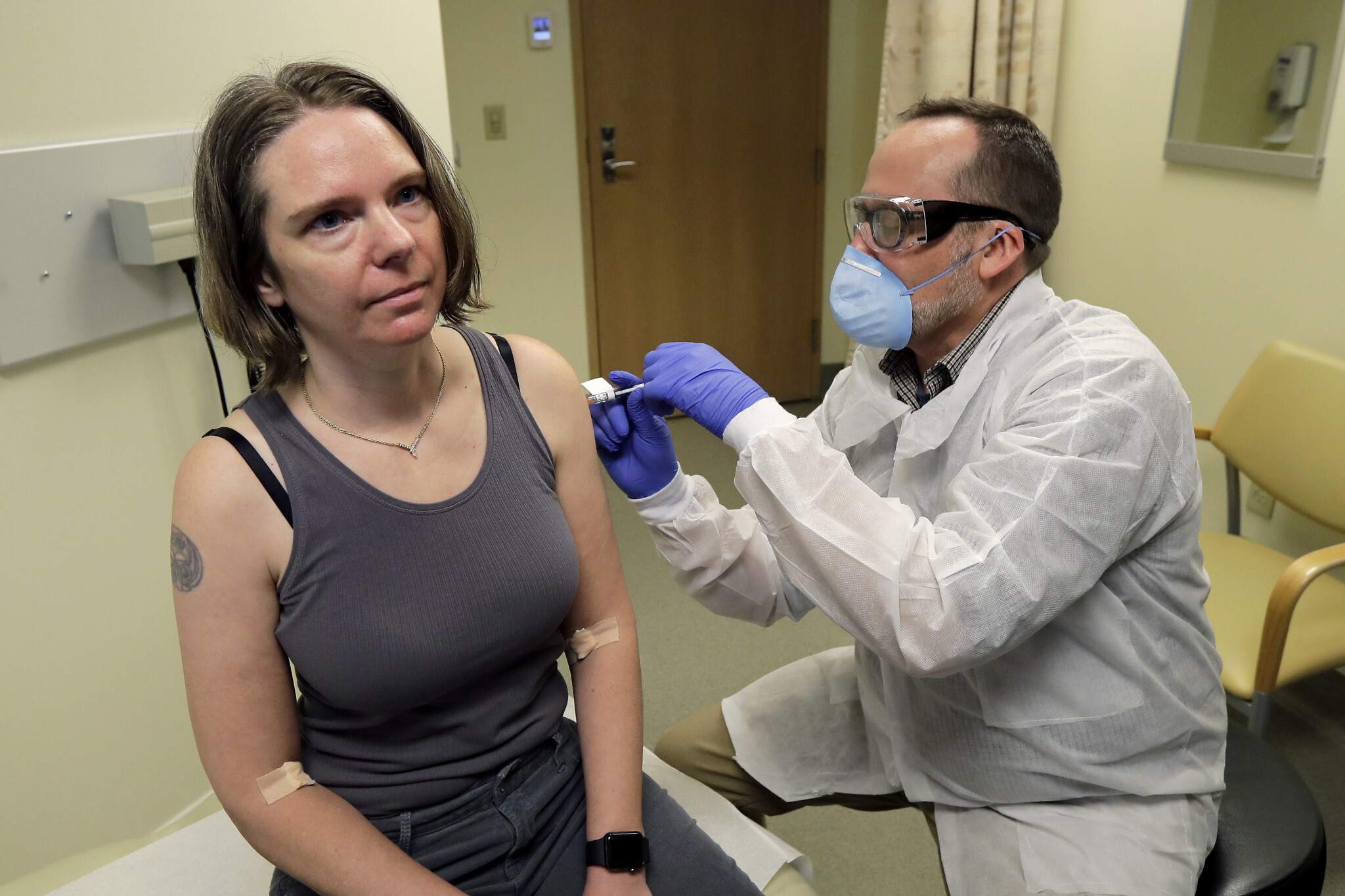
Un pharmacien donne à une volontaire, à gauche, une dose de vaccin lors d’un essai réalisé dans le cadre d’une étude clinique de Phase 1 pour un vaccin anti-COVID-19 mis au point par Moderna Inc. au Permanente Washington Health Research Institute de Seattle, le 16 mars 2020 (Crédit : AP Photo/Ted S. Warren, File)
L’essai de phase II, impliquant 600 personnes, a d’ores et déjà reçu le feu vert de la part de l’agence du médicament américaine (FDA – Food and Drug Administration). Moderna devrait le commercialiser ce trimestre.
Un essai de phase III – le plus important et le plus large pour la validation de l’efficacité d’un vaccin – débutera au mois de juillet.
« Ces données intermédiaires révélées par l’essai de phase I montrent, même si elles sont anticipées, qu’une vaccination avec le mRNA-1273 entraîne une réponse immunitaire de la magnitude causée par l’infection de manière naturelle », écrit Tai Zaks dans le communiqué de presse officiel de la firme. « Ces données renforcent nos certitudes, celles que le mRNA-1273 possède le potentiel de prévenir la Covid-19 et que nous pourrons faire les progrès nécessaires pour parvenir à sélectionner une dose pour des essais déterminants ».
Moderna, une compagnie qui a été fondée il y a neuf ans, a indiqué que le vaccin s’était avéré « sûr et bien toléré en général » et que les patients n’avaient eu à déplorer que quelques rougeurs ou courbatures à la suite de l’injection.
Lors d’une visioconférence, le directeur général de Moderna qui détient
9 % de Moderna, Stéphane Bancel, a expliqué que les tests préliminaires laissaient penser que le mRNA-1273 avait un degré élevé de protection probable » contre le virus.
9 % de Moderna, Stéphane Bancel, a expliqué que les tests préliminaires laissaient penser que le mRNA-1273 avait un degré élevé de protection probable » contre le virus.
« Nous n’aurions pas pu être davantage satisfaits de ces données intermédiaires », a commenté le Français Stéphane Bancel au sujet des essais de
phase I.
phase I.
Des tests distincts réalisés sur des souris ont montré que le vaccin avait empêché le virus de se reproduire dans les poumons, selon la firme.
Le gouvernement américain a investi presque un demi-milliard de dollars dans le développement du vaccin proposé par Moderna.
Ce développement s’effectue en partenariat avec l’Institut national des Allergies et des maladies infectieuses, placé sous l’autorité d’Anthony Fauci, et les essais cliniques ont été réalisés par les Instituts nationaux de Santé.
« L’équipe de Moderna continue à se consacrer à avancer aussi rapidement et de la manière la plus sûre possible pour pouvoir lancer l’étude déterminante de phase III au mois de juillet », a continué son directeur général.
Sur la base des résultats partiels de la phase I, Moderna a indiqué qu’elle n’étudiera plus les doses de vaccin les plus élevées dans la mesure où les plus minimes semblaient faire effet.
« Plus basse sera la dose, plus nombreux seront les gens que nous nous attendons à pouvoir protéger », a fait savoir le président de Moderna, Stephen Hoge.
Le président Donald Trump a fait savoir qu’il voulait 300 millions de doses de vaccin d’ici le mois de janvier 2021 pour pouvoir protéger la population américaine, et son administration a accordé des financements à Moderna, Johnson & Johnson ainsi qu’au français Sanofi.
Le développement d’un vaccin prend habituellement des années mais la pandémie de coronavirus, qui a déjà entraîné plus de 315 000 morts, a donné un caractère d’urgence sans précédent aux recherches.
Une dizaine d’essais cliniques sont déjà en cours dans le monde entier, selon la London School of Hygiene & Tropical Medicine de Londres.
La Chine, pour sa part, a déclaré mener des essais sur les êtres humains dans le cadre de cinq vaccins expérimentaux.
Le défi n’est pas seulement de trouver un vaccin sûr et efficace, mais également d’en produire des millions de doses.
Plusieurs laboratoires importants – dont Moderna – ont indiqué qu’ils lanceraient immédiatement la production d’un éventuel vaccin, même avant la fin de tous les essais cliniques.
Moderna a récemment annoncé un partenariat avec le géant pharmaceutique Lonza qui permettra d’augmenter ses capacités de production à un milliard de doses par an.
Il existe actuellement, dans le monde entier, une dizaine de vaccins dont les essais viennent de commencer ou débuteront bientôt. Les responsables de la santé ont estimé que si tout se passait bien, ces études pourraient s’achever dès la fin de l’année, voire au début de l’année prochaine.
Plus de 4,7 millions de cas de contamination au coronavirus et 315 000 décès ont été enregistrés dans le monde depuis l’apparition du virus en Chine, à la fin de l’année dernière. Aucun traitement spécifique n’a encore été approuvé, même si plusieurs ont été utilisés en urgence après s’être révélés prometteurs au cours d’essais préliminaires.



Aucun commentaire:
Enregistrer un commentaire